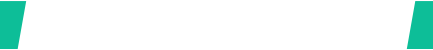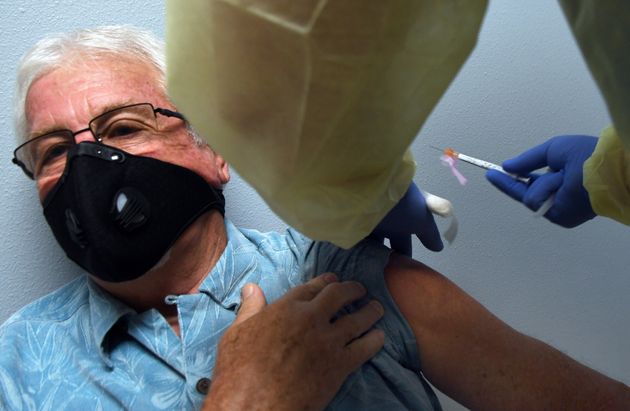
미국 질병통제예방센터(CDC)가 50개주와 5개 대도시 보건당국에 10월 말 또는 11월 초부터 코로나19 백신 접종을 개시할 수 있도록 준비하라는 지침을 내려보냈다고 뉴욕타임스(NYT)가 2일(현지시각) 보도했다.
CDC는 이 지침에서 두 개의 백신 후보물질을 언급하며 아직은 ‘가정’일 뿐이라는 단서를 달았다. 그러나 트럼프 정부가 11월3일 대선에서 유리한 국면을 조성하기 위해 검증이 덜 끝난 백신을 서둘러 출시할 수 있다는 우려가 제기되어 온 터라 논란이 이어질 것으로 보인다.
CDC의 코로나19 백신 가이드라인
NYT가 입수해 보도한 세 장의 문건(문서1, 문서2, 문서3)에 따르면, CDC는 ”제한적인 수량의 코로나19 백신이 2020년 11월 초까지 확보될 수 있다”며 특정되지 않은 두 개의 코로나19 백신 후보물질을 우선 접종 대상자들에게 배포하는 가상의 시나리오를 언급했다.
NYT는 문건에 ‘백신 A’와 ‘백신 B’로 지칭된 백신 후보물질이 각각 화이자(Pfizer)와 모더나(Moderna)가 개발 중인 백신으로 보인다고 전했다.
우선 CDC는 의료진과 요양원 직원, 국가안보나 교육, 식품 분야 등에 종사하는 필수인력, 65세 이상과 소수인종 등 코로나19 고위험군으로 알려진 사람들을 우선 접종 대상으로 꼽았다. 이어 각각의 백신의 수송 및 보관 방법(냉동 보관)과 접종 주기(몇주 간격으로 2회 접종) 등을 구체적으로 설명했다.
CDC는 또 2009년 신종플루(H1N1) 유행 당시 초기에 백신 공급이 수요를 충분히 따라가지 못했던 일을 언급하며 각 지역의 보건당국이 만반의 준비태세를 갖춰야 한다고 덧붙였다. 병원과 이동 진료소, 그밖의 시설 등 우선 접종 대상자들에게 차질 없이 백신이 접종될 수 있도록 미리 대상자 규모를 파악하고, 접종 시설을 확보하는 등의 계획을 세우라는 얘기다.

전문가들의 우려 : ‘너무 촉박한 것 같다’
버지니아대의 폐질환 전문의 타이슨 벨 박사는 ”병원과 의료기관들이 준비할 수 있도록 계획을 마련하는 건 좋은 일”이라면서도 문건에 언급된 일정이 ”대단히 야심만만하다”고 지적했다. ”정부가 과학을 따르기보다는 (11월3일이라는) 임의의 시한을 우선시 할 것이라는 우려”가 든다는 얘기다.
베일러의대의 세드릭 다크 박사는 ”백신이 전부 고소득층 부유한 교외지역으로 쏠리지 않도록” CDC가 필수 인력과 고위험군 취약 계층 등에 대한 백신 우선 공급 계획을 세운 것은 다행이라면서도 일정이 너무 촉박한 것 같다고 말했다. “10월이면 30일 정도 밖에 안 남았다.”
현재 화이자와 모더나는 각각 3만명의 참가자들을 대상으로 3상 임상시험을 진행하고 있다. 이같은 대규모 임상시험을 통해 안전성과 유효성(효과) 검증이 끝난 다음 백신을 출시하는 게 일반적인 절차다.
특히 어느 특정 인구집단에서 부작용이 나타날 수 있기 때문에 막대한 시간과 비용이 소요되더라도 대규모 임상시험은 필수다. 원래 일정대로라면 두 업체의 임상시험은 연말이나 되어야 완료될 예정이다.

대선 전 백신 출시 무리수?
그러나 최근 미국 보건당국자들은 3상 임상시험이 완료되기 전이라도 코로나19 백신을 승인할 수 있다고 밝혀왔다. 스티븐 한 식품의약국(FDA) 국장은 지난주 파이낸셜타임스(FT) 인터뷰에서 ”(임상시험이 덜 끝난 백신의) 이득이 위험보다 훨씬 더 크다(고 판단될 때)” 긴급사용승인(EUA)을 내릴 수 있다고 말했다.
미국 감염병 최고 권위자인 앤서니 파우치 박사도 보건의료매체 KHN 인터뷰에서 비슷한 취지의 언급을 했다. 그는 임상시험 초기에 안전성과 유효성에 대한 ‘압도적으로 긍정적인’ 결과가 나올 경우 조기에 임상시험을 종료하는 게 ”도덕적 의무”일 것이라고 말했다.
파우치 박사는 과학자들로 구성된 위원회가 오직 객관적 증거와 임상시험 결과 자료에 따라 임상시험 조기 종료 여부 등을 결정할 것이라고 덧붙였다. ”정치적 압력에 대해서는 우려하지 않는다”는 것.
반면 전염병 예방학자 사스키아 포페스쿠는 “10월 말까지라는 이 (백신) 보급 일정은 공중보건의 정치화, 안전성 문제가 있을 수 있다는 점에서 깊이 우려스럽다”고 NYT에 말했다. ”선거 전 백신 (보급)을 밀어부치기 위한 게 아니라고 보기는 어렵다.”